Термодинамика

Термодинамиката е физичка дисциплина што ги изучува својствата на топлинската енергија и нејзините трансформации. Поделена е на рамнотежна термодинамика и нерамнотежна термодинамика. Рамнотежната термодинамика ги изучува системите што се во состојба на стационарна термодинамичка рамнотежа, додека нерамнотежната термодинамика ги изучува оние системи што не се во состојба на термодинамичка рамнотежа.
Кога зборуваме за термодинамиката, вообичаено се мисли на феноменлошката термодинамика која термодинамичките системи ги изучува феноменолошки, односно со воопштување на експерименталните резултати и не водејќи сметка за микро карактеристиките на системите. Законитостите во термодинамиката се засновани на термодинамичките принципи.
Во термодинамиката, термодинамички систем, првично наречен работна супстанца, се дефинира како оној дел од вселената на кој сме сосредоточени. Една хипотетичка граница го одделува овој систем од останатиот дел на вселената, наречен околина или резервоар. Многу корисна е класификацијата на термодинамичките системи која се основа на природата на границата и величините кои протекуваат низ неа, како што се материја, енергија, работа, топлина и ентропија. Систем може да биде било што, на пример раствор во епрувета, жив организам, електрична мрежа, планета итн.
Во изолираните системи е забележано дека со тек на времето, внатрешните преуредувања (заемодејства) постепено исчезнуваат и се доаѓа до една блиску-стабилна состојба. Притисоците и температурите тежнеат да се изедначат, додека материјата се распоредува во неколку релативно хомогени агрегатни состојби. Систем во кој сите процеси на измена дошле практично до својот крај се смета дека е во состојба на термодинамичка рамнотежа. Термодинамичките својства на системот во рамнотежа не се менуваат со времето. Рамнотежните системи се многу полесни за опишување на детерминистички начин, за разлика од оние кои не се во рамнотежа.
При термодинамичките процеси, големите отстапувања од рамнотежната состојба за време на интермедиерните чекори се резултат на зголемувањето на ентропијата и производството на повеќе топлина наместо корисна работа. Може да се покаже дека за да еден процес биде повратен, тогаш секој чекор во процесот мора да е повратен. За да еден чекор од даден процес биде повратен, системот мора да биде во рамнотежа за време на одвивањето на чекорот. Оваа идеална состојба не може да се постигне во пракса, бидејќи ниеден чекор не може да се одвива без нарушување на рамнотежата во системот, но може приближно да се дојде до неа со постепено (бавно) одвивање на промените во системо
Во отворените системи, материјата може да навлегува и излегува од границата на системот. Првиот закон на термодинамиката за отворени системи гласи: зголемувањето на внатрешната енергија на еден систем е еднаква на количината енергија додадена на системот преку проток на материја во него и со загревање, минус количината на изгубена материја во форма на работа обавена од страна на системот.
Термодинамиката (од грчки: θέρμη, топлина и δύναμις, сила; буквално може да се преведе како топлосила) е клон на природните науки (основно физика и химиа), се занимава со топлинските процеси, протекува во телата пропратено со промена на температурата, големината , условите и врската со други форми на енергија и работа.
Термодинамика е наука која ги проучува појавите настанати од меѓусебното претворање на топлината и другите форми на енергија (механички, хемиски, електрични).
Искуствено се знае дека од механичка работа се добива топлина .
Ние знаеме дека на пример со триење, механичката енергија се претвора во топлина (добивање на огнот во старите времиња). Оваа пренамена е релативно лесно и целосно, што значи дека сите трудот вработени се претвора во топлина.
Познато е исто така дека топлината може да се конвертира во механичка работа.
Херон Александриски приметил дека водата со загревање врие и испарува претворајќи се во пареа која може да врши работа.
Сепак, конверзијата на топлина во работа не е лесна и едноставна и тоа никогаш не е потполнана.
Решението на претворањето работата во топлина и топлината во механичка работа, доведе до термодинамиката како наука. До тоа дошло од емпириски знаења и практични потреби, отколку од теоретски размислувања.
Топлината се дефинира како енергија во преод која се регистрира (чувствува) и пренесува како резултат на температурната разлика. Топлината секогаш поминува од потопло на постудено тело, така што насоката на распространување е одредена со природен закон (вториот закон на термодинамиката).Топлина е движењето на топлинската енергија од еден предмет со повисока температура на предмет со пониска температура.
Шкотскиот физичар Џејмс Клерк Максвел, во неговото класично дело “Теорија на топлината“ од 1871 г., бил еден од првите кој се обидел да даде модерна дефиниција за топлина. Главно, Максвел истакнува четири одредби за дефинирање на топлината. Првата, дека тоа е “нешто што може да се префрли од едно тело на друго, што го претставува Вториот закон на термодинамиката. Второ, дека таа може да се смета за “мерлива големина“ и затоа може да се третира математички како останатите мерливи големини. Трето, таа “не може да се третира како супстанца“; таа може да се трансформира во нешто што не е супстанца, на пример, механичка работа. Најнакрај, таа е “една од формите на енергијата“.
Топлината се означува со Q, а СИ-единица за топлина е џул (J). Кога температурите ќе се изедначат, топлината е еднаква на нула. Топлината исклучиво е поврзана за преодот, па таа е процесна големина.
Конвенција за преод на топлина:
ΔQ > 0 - ако топлината му е предадена на системот
ΔQ < 0 - ако системот ја предал топлината на околината
Топлината се пренесува со кондукција, конвекција и зрачење.
Енергија
Енергијата представува збир на сите движења што може да ги има едно тело(материја).Движењата можат да бидат
1.Видливи(макрo) или надворешни и
2.Невидливи(микро) кои ги прават молекулите како најситни честички што ги задржале особините на материјата.Во невидливи движења спаѓаат и движењата на атомите.Оваа енергија се натекува атомска енергија.Збирот на енергиите на молекулите и атомите се нарекува внатрешна енергија.
Движењата на телото може да бидат изразени како А) травслација и Б)ротација.
Надворежната енергија може да биде енергија на положбата или потенцијална енергија и енергија на движење или кинетижна енергија.Збирот на кинетичката и потенцијалната енергија со заедничко име се нарекува механичка енергија.Овој збир секогаш е константен по физичкиот закон за зачувување на механичката енергија. Раликата на енергијата меѓу две нивоа(почетно и крајно) се нарекува работа.
Внатрешната енергија е кинетичка енергија на молекулите и може да биде изразена како притисна енергија и топлина.
1.Видливи(макрo) или надворешни и
2.Невидливи(микро) кои ги прават молекулите како најситни честички што ги задржале особините на материјата.Во невидливи движења спаѓаат и движењата на атомите.Оваа енергија се натекува атомска енергија.Збирот на енергиите на молекулите и атомите се нарекува внатрешна енергија.
Движењата на телото може да бидат изразени како А) травслација и Б)ротација.
Надворежната енергија може да биде енергија на положбата или потенцијална енергија и енергија на движење или кинетижна енергија.Збирот на кинетичката и потенцијалната енергија со заедничко име се нарекува механичка енергија.Овој збир секогаш е константен по физичкиот закон за зачувување на механичката енергија. Раликата на енергијата меѓу две нивоа(почетно и крајно) се нарекува работа.
Внатрешната енергија е кинетичка енергија на молекулите и може да биде изразена како притисна енергија и топлина.
Работно тело
Специфичен волунен на гасовите
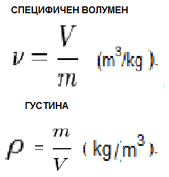
Волуменот е физичка големина и го представува просторот што го зафаќа материјата.Волуменот на гасовите е простор што го зафаќа садот во кој се наоѓа одредено количество гас.
Волуменот што го зафаќа единица маса гас при одредени услови се нарекува специфичен волумен
Реципрочната вредност на специфичниот волумен представува густина на гасот.
Волуменот што го зафаќа единица маса гас при одредени услови се нарекува специфичен волумен
Реципрочната вредност на специфичниот волумен представува густина на гасот.
Притисок на гасовите
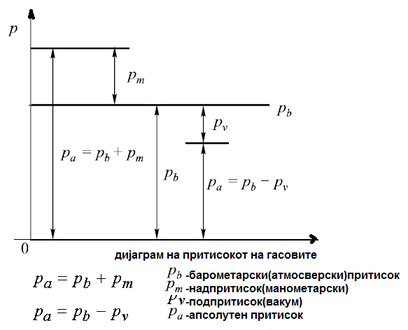
Притисокот на гасовите е дејство на сила врз површините на садот во кој се наоѓа гасот. p=F/A (N/mm2)
Притисокот на околината се нарекува атмосверски или барометарски и се мери со барометар.
Ако притисокот на гасот во садот е помал од барометарскиот тој се нарекува подпритисок или вакум и се мери со вакумметар.
Ако притисокот на гасот во садот е поголем од барометарскиот тој се нарекува надпритисок и се мери со манометар
Во праксата се работи со т.н. апсолутен притисок.Неговата големина се пресметува,но не може да се отчита на иструментите(вакумметар,манометар)
Притисокот како физичка големина е изведена големина и во интернационалниот систем на мерни единици се мери во Pa(паскал)
Најчесто се сретнува единицата hPa(хекто паслал),аво техниката 1 bar(бар)
1 bar- 100000 Pa
Притисокот на околината се нарекува атмосверски или барометарски и се мери со барометар.
Ако притисокот на гасот во садот е помал од барометарскиот тој се нарекува подпритисок или вакум и се мери со вакумметар.
Ако притисокот на гасот во садот е поголем од барометарскиот тој се нарекува надпритисок и се мери со манометар
Во праксата се работи со т.н. апсолутен притисок.Неговата големина се пресметува,но не може да се отчита на иструментите(вакумметар,манометар)
Притисокот како физичка големина е изведена големина и во интернационалниот систем на мерни единици се мери во Pa(паскал)
Најчесто се сретнува единицата hPa(хекто паслал),аво техниката 1 bar(бар)
1 bar- 100000 Pa
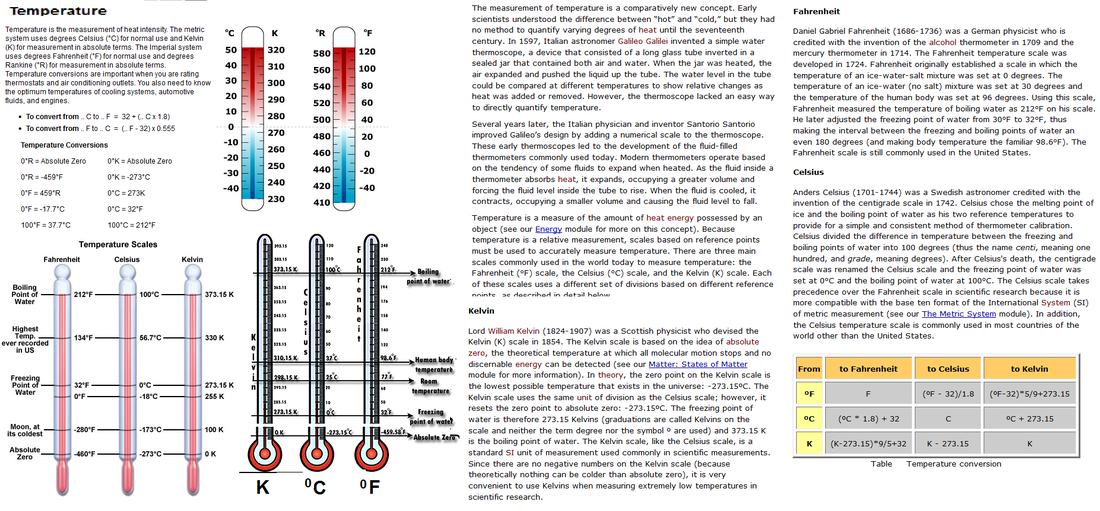
Температура
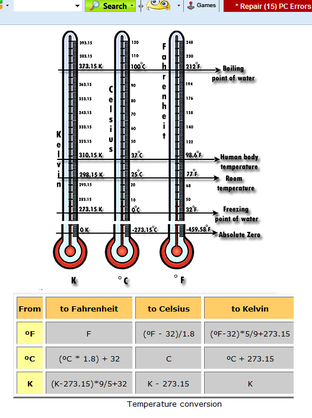
Температурата е внатрешна големина на состојбата на гасовите која го покажува степенот на нивната загреаност,и ја карактеризира нивната толинска состојба.
Ако имаме два сада со гас од кои едниот е потопол а другиот поладен и ако се допрат еден до друг ќе забележиме дека потоплиот сад се лади а поладниот се загрева се додека не се изедначат нивните температури.Во тој момент кажуваме дека двата сада се во топлинска рамнотежа,и имаат иста термпература.
Температурата не зависи од видот на материјата,нејзината маса,волумен и притисок.
Промената на температурата на телата предизвикува најразлични промени.(промена на димензиите,агрегатната состојба,електричен отпор,физички и хемиски особини)
Промената на температурата се објаснува преку кинетичко молекуларната теорија.Со промена на брзината на движење на молекулите се менува кинетичката енергија која поради промената на судирањето на молекулите и нивното меѓусебно триење се превора во топлина која се манифестира со промена на температурата.
Температурата е споредбена величина. Се мери со термометар а се изразува преку температурни скали.Најпознати температурни скали се:
1.Целзиусова
2.Фаренхајтова
3.Реомирова.
Во интернационалниот систем на мерни единици температурата е основна големина со единица мера 1К(Келвин),изразена преку Келвинова температурна скала(Термодинамичка топлинска скала)
На оваа скала нема негативна температура.Големината 0 К се нарекува апсолутна нула
Состојбата при температура од 0 К се нарекува термодинакичка смрт бидејќи не постои никакво движење на молекулите од материјата.
Температурата представена преку термодинамичката топлинска скала се нарекува апсолутна температура.
Математички таа се пресметува преку изразот: Т =t + 273,15 К
t(oC)- температура изразена во целзиусова скала
273,15 - е вредност која одговара на t=0 oC
Големината еден степен целзиусов е големина која оговара на стоти дел од разликата меѓу температурата на мрзнење на водата 0 oC и температурата на вриење на водата 100 oC
Ако имаме два сада со гас од кои едниот е потопол а другиот поладен и ако се допрат еден до друг ќе забележиме дека потоплиот сад се лади а поладниот се загрева се додека не се изедначат нивните температури.Во тој момент кажуваме дека двата сада се во топлинска рамнотежа,и имаат иста термпература.
Температурата не зависи од видот на материјата,нејзината маса,волумен и притисок.
Промената на температурата на телата предизвикува најразлични промени.(промена на димензиите,агрегатната состојба,електричен отпор,физички и хемиски особини)
Промената на температурата се објаснува преку кинетичко молекуларната теорија.Со промена на брзината на движење на молекулите се менува кинетичката енергија која поради промената на судирањето на молекулите и нивното меѓусебно триење се превора во топлина која се манифестира со промена на температурата.
Температурата е споредбена величина. Се мери со термометар а се изразува преку температурни скали.Најпознати температурни скали се:
1.Целзиусова
2.Фаренхајтова
3.Реомирова.
Во интернационалниот систем на мерни единици температурата е основна големина со единица мера 1К(Келвин),изразена преку Келвинова температурна скала(Термодинамичка топлинска скала)
На оваа скала нема негативна температура.Големината 0 К се нарекува апсолутна нула
Состојбата при температура од 0 К се нарекува термодинакичка смрт бидејќи не постои никакво движење на молекулите од материјата.
Температурата представена преку термодинамичката топлинска скала се нарекува апсолутна температура.
Математички таа се пресметува преку изразот: Т =t + 273,15 К
t(oC)- температура изразена во целзиусова скала
273,15 - е вредност која одговара на t=0 oC
Големината еден степен целзиусов е големина која оговара на стоти дел од разликата меѓу температурата на мрзнење на водата 0 oC и температурата на вриење на водата 100 oC